Retaxfalle Lieferengpässe
Hinweis
Es handelt sich bei dem Inhalt dieser Seite um eine frühere Veröffentlichung. Bitte beachten Sie, dass die Aussagen gegebenenfalls nicht mehr der aktuellen Rechts- und Vertragslage entsprechen.
Bei Fragen hilft Ihnen das DAP-Team auch gerne persönlich weiter – schreiben Sie einfach eine E-Mail an insonderfo@anderesdeutschesapothekenportal.de.
Wie kann die Patientenversorgung aufrechterhalten werden, ohne dass eine Retax droht?
Lieferengpässe rücken bei der Arzneimittelversorgung immer wieder in den Fokus. Während kurzfristige Engpässe manchmal durch Abgabe anderer Packungsgrößen überbrückt werden können, sorgen länger andauernde Lieferschwierigkeiten für große Probleme bei der Patientenversorgung. Ein prominentes Beispiel war im Frühjahr/Sommer dieses Jahres der Tamoxifen-Engpass, aktuell sind Apotheken täglich mit dem Lieferengpass im Bereich der Ibuprofen- und Paracetamol-haltigen Fiebersäfte konfrontiert. Hier können Apotheken durch Rezepturherstellung die Versorgung aufrechterhalten. Durch eine Bekanntmachung des BfArM („Aktuelle Informationen des BfArM zur eingeschränkten Verfügbarkeit von Paracetamol- und Ibuprofen-haltigen Fiebersäften für Kinder“1), in der es darum geht, wie dabei vorzugehen ist, wird die Gefahr von Retaxationen weitestgehend abgefedert.
Was ist zu beachten, wenn Importe die einzige Alternative sind?
In manchen Fällen kann ein Lieferengpass durch Importarzneimittel überbrückt werden. Doch dann stellt sich die Frage, wie dabei die rechtliche Situation ist. Für Einzelimporte gelten gemäß § 73 Abs. 3 Arzneimittelgesetz (AMG) folgende Voraussetzungen:
- Bestellung für eine einzelne Person in geringer Menge
- Abgabe im Rahmen einer bestehenden Apothekenbetriebserlaubnis
- Arzneimittel in dem Staat, aus dem es nach Deutschland importiert wird, rechtmäßig in Verkehr
- Keine hinsichtlich des Wirkstoffs identischen und hinsichtlich der Wirkstärke vergleichbaren Arzneimittel für das betreffende Anwendungsgebiet in Deutschland verfügbar
- Keine Rücknahme, kein Widerruf, kein Ruhen der Zulassung in Deutschland gem. § 30 Abs. 4 AMG
- Keine Dopingsperre
- TSE-Verordnung zutreffend und erfüllt
- § 5 (Verbot bedenklicher Arzneimittel) und § 8 (Verbote zum Schutz vor Täuschung) AMG nicht betroffen
Soll ein einzeln importiertes Arzneimittel zulasten einer GKV abgerechnet werden, ist in jedem Fall für jede Verordnung vorab eine Genehmigung durch die Krankenkasse erforderlich, in der auch der Abrechnungspreis bestimmt wird. Wird diesen Vorgaben nicht entsprochen, so droht eine Retax. Ist die Versorgung aufgrund eines Lieferengpasses also nur noch durch Einzelimporte umsetzbar, so ist dies neben einem vermehrten Zeitaufwand auch mit deutlich gesteigerter Bürokratie verbunden – bis der Patient versorgt werden kann, dauert es erheblich länger als gewöhnlich. Da Lieferengpässe offensichtlich immer mehr zunehmen, sollten hier Wege gefunden werden, die eine schnelle und retaxsichere Versorgung ermöglichen.
Aktueller Vigabatrin-Lieferengpass: Erleichterte Vorgaben sichern Patientenversorgung
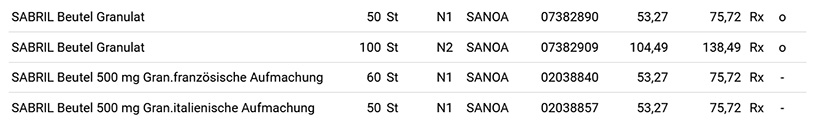
Ein weiterer Lieferengpass trifft seit Juli 2022 Vigabatrin-haltige Arzneimittel aus dem Bereich der Antiepileptika, genauer gesagt Sabril® Beutel und Sabril® 500 mg Filmtabletten. Da der Lieferengpass nach offiziellen Meldungen voraussichtlich bis zum ersten Quartal 2023 andauern kann, wird nun durch den Hersteller Sanofi italienisch und französisch gekennzeichnete Ware in den deutschen Markt gebracht. Auch dies ist ein ungewöhnlicher Vorgang und zumindest in diesem Fall wurde sichergestellt, dass Apotheken die Arzneimittel retaxsicher abgeben können:2
- Gemäß einer Ausnahmegenehmigung basierend auf der Regelung des § 4 Abs. 1 der Medizinischer Bedarf Versorgungssicherstellungsverordnung (MedBVSV) ist die ausländische Ware in Deutschland verkehrsfähig. Die entsprechende Gestattung ist auf der Seite des BfArM veröffentlicht und voraussichtlich bis 31.12.22 befristet. Der Ware wird bei der Auslieferung ein deutsches Begleitschreiben beigelegt.
- Die ausländische Ware wird zum gleichen Preis mit identischem Herstellerabgabepreis und -rabatt abgegeben und erhält eigene PZN. Seit 15.10.22 erscheinen die ausländischen Präparate auch in der Lauer-Taxe.
- Einzelimporte nach § 73 Abs. 3 AMG sind in der Regel wie oben beschrieben genehmigungspflichtig, allerdings verzichtet der GKV-Spitzenverband in diesem Fall ausnahmsweise auf die Genehmigung, um eine reibungslose Versorgung zu ermöglichen.
- Damit kann die Apotheke die ausländische Ware mittels Bedruckung der in der Taxe dargestellten PZN mit der GKV abrechnen. Zusätzlich empfiehlt sich ein Vermerk wie „Sabril-Lieferengpass“ oder Ähnliches auf dem Rezept. Diese Vorgehensweise ist vielen Apotheken vielleicht noch aus dem Jahr 2020 bekannt, als der damalige Pneumovax®-Engpass ebenfalls mit Importware aus Japan, die mit eigener PZN in der Taxe gelistet war, überbrückt wurde.
Aktueller 5-FU-Lieferengpass
Auch bei Fluorouracil-haltigen Injektionslösungen, die in parenteralen Zubereitungen zur Anwendung kommen, gibt es derzeit einen Lieferengpass. Hier wird ebenfalls mittels Sondergenehmigung durch das BfArM Abhilfe geschaffen: Es dürfen Importpräparate, die für den englischen Markt bestimmt sind, trotz englischsprachiger Kennzeichnung in Deutschland in Verkehr gebracht werden. Die Abrechnung erfolgt in diesem Fall über die in der Taxe dargestellten PZN des deutschen Präparates über den in der Hilfstaxe vereinbarten Preis. Auch der englische Import unterliegt damit den deutschen Preisregularien.3
Fazit
Um Lieferengpässe zu überbrücken und die Patienten zeitnah zu versorgen, ist in Apotheken in vielen Fällen ein erhöhter (bürokratischer) Aufwand erforderlich. Es ist wünschenswert, dass bei länger andauernden Lieferengpässen verbindliche Lösungen zur Herstellung bzw. Abrechnung vereinbart werden, damit Apotheken zumindest nicht in ein Retaxrisiko laufen, wenn sie ihre Patienten mit Alternativen versorgen.
1 https://www.bfarm.de/DE/Arzneimittel/Arzneimittelinformationen/Lieferengpaesse/mitteilung_fiebersaefte_kinder.html
2 Rundschreiben apothekerverband Schleswig-Holstein e.V. Nr. 139 vom 05.10.2022
3 Information des ABDATA Pharma-Daten-Service „Abrechnung Fluorouracil-haltige in parenteralen Zubereitungen / Gestattung des BfArM“ vom 10.10.2022
Neuen Kommentar schreiben
Sie müssen angemeldet sein, um die Kommentarfunktion nutzen zu können.
Benutzeranmeldung
Geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden
DAP Newsletter
Immer aktuell informiert mit dem DAP Newsletter: zur Newsletter-Anmeldung
