Neue austauschbare Bioidenticals
Hinweis
Es handelt sich bei dem Inhalt dieser Seite um eine frühere Veröffentlichung. Bitte beachten Sie, dass die Aussagen gegebenenfalls nicht mehr der aktuellen Rechts- und Vertragslage entsprechen.
Bei Fragen hilft Ihnen das DAP-Team auch gerne persönlich weiter – schreiben Sie einfach eine E-Mail an insonderfo@anderesdeutschesapothekenportal.de.
Nicht nur die Vorgaben zur Dosierung auf dem Rezept haben sich zum 1. November 2020 geändert, auch in Anlage 1 zum Rahmenvertrag (nach § 129 Abs. 2 SGB V) gab es eine Ergänzung: Zwei Biologicals sind neu hinzugekommen. In Anlage 1 wird definiert, welche biotechnologisch hergestellten Arzneimittel im Rahmen der Aut-idem-Regelung in der Apotheke austauschbar sind (sog. Bioidenticals).
Mit Wirkung zum 1. November 2020 wurden die Arzneimittel Cegfila (STADAPHARM) und Pelmeg (Mundipharma) in Anlage 1 zum Rahmenvertrag aufgenommen. Beide enthalten den Wirkstoff Pegfilgrastim. Als Bioidenticals können sie nun „aut idem“ ausgetauscht werden, sofern dem Austausch keine anderen Bedenken entgegenstehen und die Verordnung nicht mit Aut-idem-Kreuz ausgestellt wurde. Die Präparate fallen damit unter die Regelungen des Marktes preisgünstiger Arzneimittel nach § 12 Abs. 1 Rahmenvertrag (vorrangige Abgabe eines Rabattarzneimittels; wenn kein Rabattarzneimittel verfügbar: Abgabe eines der vier preisgünstigsten Arzneimittel).
Aktuell sind diese Bioidenticals in Anlage 1 gelistet (Stand: 01.11.2020):
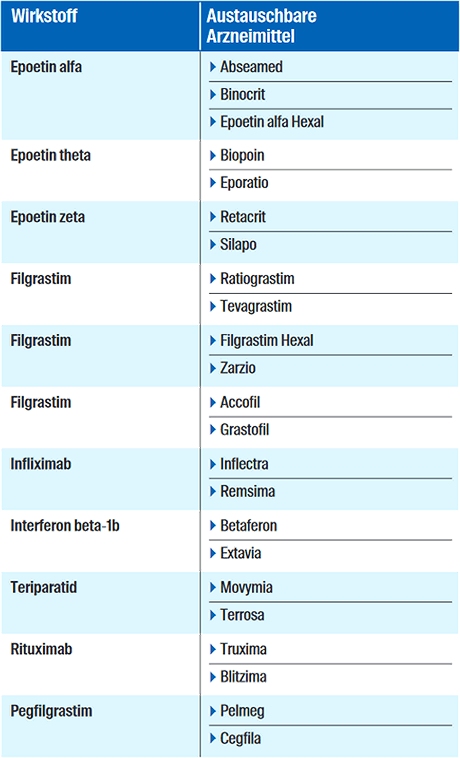
Kein Aut-idem-Austausch bei den anderen Pegfilgrastim-Präparaten
Das Original-Biologikum (Referenzpräparat) Neulasta und die anderen Pegfilgrastim-Biosimilars (Ziextenzo, Pelgraz, Grasustek, Fulphila) sind jeweils nicht untereinander austauschbar, auch nicht durch Cegfila oder Pelmeg. Obwohl sie denselben Wirkstoff enthalten, so unterscheiden sie sich dennoch in ihren Herstellungsverfahren. Somit darf bei einer Verordnung über Neulasta beispielsweise nur das jeweilige Original oder ein zugehöriger Import abgegeben werden. Gleiches gilt für alle anderen Biosimilars (mit Ausnahme von Cegfila und Pelmeg): auch hier steht jeweils nur das Original oder ein zugehöriger Import zur Abgabe zur Verfügung.
Hintergrund
Biotechnologisch hergestellte Arzneimittel dürfen in der Apotheke nur dann aut idem substituiert werden, wenn sie in Anlage 1 gelistet sind. Geregelt ist dies in § 9 Abs. 3 Rahmenvertrag. Bei allen anderen Biologika ist eine Aut-idem-Substitution nicht zulässig und nur ein Austausch zwischen Original- und Importarzneimitteln erlaubt. Bioidenticals sind biotechnologisch hergestellte Arzneimittel, die aus derselben Produktionsstätte stammen und daher identisch und damit auch untereinander austauschbar sind. Es muss allerdings berücksichtigt werden, ob ein Unterschied hinsichtlich Handhabung und Applikation besteht.

