Biologicals nach Anlage 1 Rahmenvertrag – ist ein Austausch zwingend erforderlich?
Hinweis
Es handelt sich bei dem Inhalt dieser Seite um eine frühere Veröffentlichung. Bitte beachten Sie, dass die Aussagen gegebenenfalls nicht mehr der aktuellen Rechts- und Vertragslage entsprechen.
Bei Fragen hilft Ihnen das DAP-Team auch gerne persönlich weiter – schreiben Sie einfach eine E-Mail an insonderfo@anderesdeutschesapothekenportal.de.
Uns liegt ein Rezept zulasten der AOK vor, auf dem „Abseamed 2000 N3 PZN 04000652“ verordnet wurde.
Unsere Software zeigt uns danach die Tabelle der Generika mit den preisgünstigen Importen, z. B. Binocrit von EMRAmed, Orifarm und EurimPharm. Ein Rabattvertrag besteht nicht.
Müssen wir Binocrit abgeben, da Abseamed in der Tabelle der Anlage 1 des Rahmenvertrags steht? Oder ist der Austausch nicht erforderlich, da es sich um ein Biological handelt? Bisher haben wir in solch einem Fall.
Antwort
Bezüglich des Wirkstoffs Epoetin alfa sind die Präparate Abseamed, Binocrit und Epoetin alfa Hexal untereinander austauschbar – dies ist in Anlage 1 des Rahmenvertrags festgehalten.

Ist eines dieser Produkte verordnet, dann gelten die Abgaberegeln nach §§ 11 und 12 des Rahmenvertrags.
Ist kein Rabattartikel (§ 11) vorrangig abzugeben, muss gemäß § 12 eines der vier Preisgünstigsten abgegeben werden:
12 Rahmenvertrag
„(1) Ist eine vorrangige Abgabe rabattbegünstigter Fertigarzneimittel nach § 11 nicht möglich, ist eines der vier preisgünstigsten Fertigarzneimittel abzugeben, das die Kriterien nach § 9 Absatz 3 erfüllt.“
In § 9 findet man dann den Hinweis, dass auch die Biologika der Anlage 1 nach den Abgaberegeln des Rahmenvertrags zu beliefern sind:
9 Abs. 3 Rahmenvertrag
„a) [...] die Verpflichtung der Apotheke zur Berücksichtigung dieser Arzneimittel bei der Auswahl besteht für in Anlage 1 in der jeweils gültigen Fassung als untereinander wirkstoffgleich aufgeführte Arzneimittel.“
Auch sind die in der Anlage 1 genannten Biologika unabhängig von ihrer gemeldeten Darreichungsform austauschbar:
9 Abs. 3 Rahmenvertrag
„d) […] die in Anlage 1 genannten wirkstoffidentischen biotechnologisch hergestellten Arzneimittel mit gleicher Darreichungsform laut Punkt 3 der Fachinformation sind unabhängig von der im Preis- und Produktverzeichnis gemeldeten Darreichungsform austauschbar[.]“
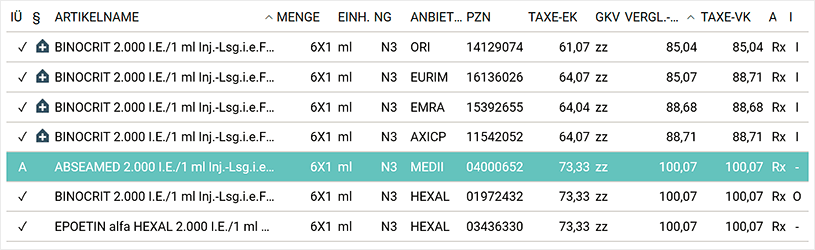
Daher ist eines der vier preisgünstigsten wirkstoffidentischen biotechnologisch hergestellten Arzneimittel abzugeben, was in Ihrem Fall wirklich vier Importe sind.
Die Möglichkeit, Pharmazeutische Bedenken geltend zu machen, haben Sie natürlich immer. Sie sollten nur auch begründbar sein – bei Bioidenticals sind ja die Präparate in Ausgangsstoffe und Herstellungsprozess identisch. Allerdings können natürlich durch abweichendes Aussehen/unterschiedliche Namen je nach Patient Probleme denkbar sein. Pharmazeutische Bedenken sind dann auf dem Rezept durch Sonder-PZN plus passenden Faktor sowie Begründung auf dem Rezept, abgezeichnet mit Datum und Kürzel, zu dokumentieren.
Weiterführende Links:
- DAP-Rubrik Biologicals
- DAP Lexikon
- Diskutieren Sie Ihre Abgabefragen auch im DAP Forum!
Anmerkung
Die Beantwortung der Fragen erfolgt im Rahmen kollegialer Hilfe.
Trotz größter Sorgfalt können wir aufgrund der teils komplizierten Sachverhalte keine Haftung übernehmen.
Neuen Kommentar schreiben
Sie müssen angemeldet sein, um die Kommentarfunktion nutzen zu können.
Benutzeranmeldung
Geben Sie Ihren Benutzernamen und Ihr Passwort ein, um sich an der Website anzumelden
DAP Newsletter
Immer aktuell informiert mit dem DAP Newsletter: zur Newsletter-Anmeldung
